انواع خوردگی شیمیایی
زنگ زدن اغلب در قسمتی از فلز اتفاق می افتد که تحت کشش و فشار (خم شدن
یا جوش خوردگی) باشد و یا در مقابل هوا عایق بندی نشده باشد. (زمانی که دو تکه
فلز به هم وصل می شوند یا یک لایه رنگ به صورت شل روی فلز قرار گرفته است).
یا جوش خوردگی) باشد و یا در مقابل هوا عایق بندی نشده باشد. (زمانی که دو تکه
فلز به هم وصل می شوند یا یک لایه رنگ به صورت شل روی فلز قرار گرفته است).
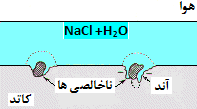
یون های فلزی در لایه رطوبت موجود روی فلز حل می شوند. و الکترون ها توسط یک
خنثی کننده به مکان دیگری مهاجرت می کنند.
اکسیژن، رایج ترین خنثی کننده است. یون های هیدروکسید تولید شده از این فرایند،
با Fe[SUP]٢+[/SUP] واکنش می دهند تا ترکیبی از اکسیدهای آهن آب دار به نام " زنگ" تشکیل
دهند.
اینکه هرکدام از قسمتهای فلز نقش کاتد یا آند را ایفا کند، به عوامل مختلفی بستگی
دارد؛ همان طور که از شکل های مختلف و بی شکل پوسیدگی، در اطراف خود متوجه
می شویم، اتم ها در مناطقی که تحت فشار باشند، اغلب تمایل دارند انرژی های آزاد
بالاتری داشته باشند و بنابراین دوست دارند آندی شوند.

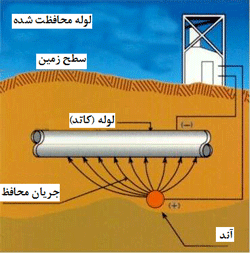
اگر قسمتی از جسم فلزی در برابر هوا محافظت شود و اکسیژن کافی برای تشکیل
یا باقی ماندن لایه اکسید وجود نداشته باشد، این ناحیه ی " محافظت شده" معمولا
قسمتی خواهد شد که در آن جا پوسیدگی فعال نیست.
مایعاتی مانند بارانهای اسیدی، آب دریا و افشانه نمکی که برای ذوب کردن برف جاده
های یخی به کار می رود، به علت ترکیبات موجود در آن ها الکترولیت های قوی تری
نسبت به آب هستند.
به همین دلیل آهن و فلزات دیگر در این محیط ها با سرعت بیش تری زنگ زده و خورده
می شوند.
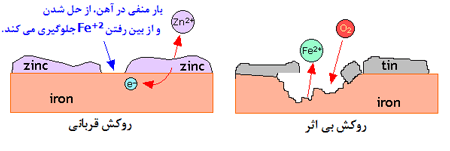
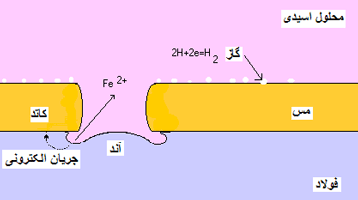
به عنوان یک مثال از یک سلول زنگ زده؛ روکشی ناکامل از مس را، روی فولادی که
در اسید سولفوریک رقیق غوطه ور شده است، می کشیم.
جریان تولید شده با کم ترین مقاومت، از مس به فولاد شارش پیدا می کند و با عبور
از یون های موجود در محلول دوباره به مس برمی گردد.
فولاد که بزرگ ترین پتانسیل منفی را دارد، حل شده و نقش آند را ایفا می کند؛ در
حالی که مس نقش کاتد را ایفا می کند.
در چنین حمله ی اسیدی، هیدروژنی که هنگام حل شدن فولاد (که ترکیبات آهن را
در خود دارد) آزاد می شود، روی سطح کاتد مسی می نشیند و در همان حالت که
مقدار آن زیاد می شود، ممکن است دو اتفاق بیفتد:
زنگ زدگی فولاد هم به دلیل تشکیل الکترود هیدروژن با بار مخالف کم میشود (یعنی
سلول قطبی می شود) و هم ممکن است هیدروژن به صورت حباب هایی که خارج
می شود، در بیاید و در نتیجه آن زنگ زدگی به صورت پشت سر هم اتفاق خواهد
افتاد.
در حالت اول، اگر فلز در معرض عامل های اکسایشی مانند هوا قرار گیرد، زنگ زدن
سرعت بیش تری پیدا خواهد کرد که باعث گرفتن هیدروژن از کاتد می شود. اندازه
کاتد نسبت به آند مهم است مثلا اگر مس به ورق فولادی بزرگی پرچ شود، بسرعت
قطبی می شود و مقدار زنگ زدگی کم خواهد بود. از طرف دیگر، کاتد بزرگ متصل به
آند، اثر معکوسی خواهد داشت و حمله سریعی روی آند و خورده شدن آن خواهد
داشت.
آهن و فولاد رایج ترین مواد برای ساخت و ساز هستند و خاصیت زنگ خوردگی این مواد
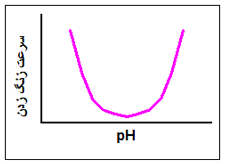
در آبهای خنثی مهم است. وقتی فولاد زنگ می زند، سرعت زنگ زدن آن معمولا توسط
واکنش کاتدی کنترل می شود و اکسیژن در این فرایند، عامل مهمی است.
در آبهای خنثی که اکسیژن حل شده آزاد ندارند، زنگ زدگی بسیار جزئی است.حضور
اکسیژن حل شده در آب، واکنش کاتدی را سریع تر می کند و در نتیجه، سرعت زنگ زدن
متناسب با مقدار اکسیژن موجود برای پخش به کاتد افزایش می یابد. از آن جا که پخش
اکسیژن، عامل کنترل کننده است، سرعت زنگ زدن با افزایش دما نیز زیاد می شود.
در آب های اسیدی (pH <٤) زنگ زدن می تواند حتی بدون حضور اکسیژن نیز اتفاق
بیفتد.
زنگ زدگی حفره ای یا شکافی:بیفتد.
زنگ زدن الکتروشیمیایی تنها از تفاوت های سطحی فلزات به وجود نمی آید، بلکه از
تغییرات خود الکترولیت نیز می تواند ایجاد شود. این پدیده چنین مکانیسمی می تواند
داشته باشد:
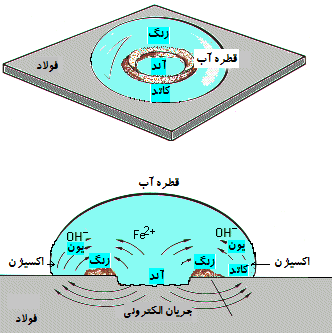
وقتی اکسیژن روی سطح آب پخش می شود، غلظت آن در جاهای مختلف قطره آب
فرق خواهد کرد؛در انتهای قطره آب، بیشترین مقدار و در مرکز قطره که آند در آن نقطه
تشکیل می شود، کم ترین مقدار را خواهد داشت.
حفره های موجود در سطح فلز و خود سطح فلز که با مواد دیگری روکش می شوند،
بیش تر در معرض چنین حملات زنگ زدگی قرار دارند.
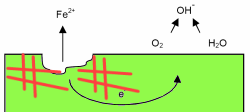
اکسیژن نمی تواند در حفره ها یا شکافها پخش شود، به همین دلیل این نقاط آندی
می شوند و کمبود اکسیژن خواهند داشت. این یون های فلزی در حفره تشکیل شده
و به بیرون مهاجرت می کنند و با یون های هیدروکسید مقابل خود واکنش می دهند
تا در دهانه حفره یا شکاف، زنگ تشکیل دهند.
مکان زنگ زدگی با پخش اکسیژن به قسمت آندی،رابطه دارد و اگر قسمت کاتدی بزرگ
باشد، ممکن است زنگ زدگی حفره ای اتفاق بیفتد. هم چنین زمانی که قسمتهای
خشک فلز در حفره ها به دام بیفتد، زنگ خوردن حفره ای می تواند رخ دهد.

موادی که در مقابل زنگ زدن بسیار مقاومند و لایه اکسیدی تشکیل شده سطحی
بر روی آن ها، از خوردگی این مواد جلوگیری می کند.(مانند فولاد) متحمل خوردگی
های حفره ای خواهند شد. این مواد، لایه اکسیدی خود را (که از وضعیت قبل از
زنگ زدن باقی مانده) نگه می دارند. زمانی که اکسیژن نمی تواند به این مواد نفوذ
کند و لایه اکسیدی شکسته می شود، سطح فلز فعال شده و ماده زنگ زدن می
شود.